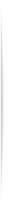RNAGEM RNA提取试剂盒
【产品简介】
RNAGEM是一种快速RNA提取试剂盒:
-
温控单管提取技术,获取样本中全部RNA
-
利用广谱特异性嗜热蛋白酶,能完整提取少量细胞的总RNA,用于基因表达谱分析
-
在15分钟内裂解细胞,降解RNA酶,从而稳定RNA
-
适用于从细胞、组织、昆虫、细菌和病毒中提取总RNA,包括miRNA,mRNA等
-
显著降低病原体环境暴露、交叉污染等人为操作失误的风险
-
不使用刺激性化学品或核酸纯化步骤
-
自动化提取(仅使用热循环仪/水浴锅)
-
适用于从载玻片/24/96/384/1536孔板中高通量提取
-
提取的核酸与大多数下游应用兼容(qPCR, RT-PCR, cDNA合成,,LAMP, Nanostring, RNAseq, scRNA-seq).
大多数RNA提取试剂盒采用固相载体纯化或有机溶剂萃取沉淀法。常见的细胞裂解缓冲体系含有后续分析反应抑制剂,如SDS,因此核酸提取后必须进行核酸纯化。核酸纯化涉及一系列实验操作,如果使用固相吸附或有机溶剂萃取法,则会损失样本RNA,显著降低RNA产量,在基因表达分析中引入偏。RNAGEM的单管提取技术解决了这个挑战,能在几分钟而不是几小时内提取高质量的核酸,而无需纯化步骤。
【RNAGEM原理和工作流程】
RNAGEM是一种快速的单管式核酸提取技术,意味着样本中所有的核酸都被完整保留,所获得的总核酸(RNA和DNA)与原始细胞数量呈现良好的线性关系。该方法是一种自动化的核酸提取技术,不需要进一步纯化,RNA可直接用于下游分析。RNAGEM试剂能够快速、有效地裂解细胞,水解核酸酶和蛋白质,充分释放出游离核酸,RNAGEM的提取产物尽可能贴近生理基因表达水平。因此,RNAGEM获得了更高的检测敏感度,尤其适用于低丰度转录本分析和痕量起始样本的分析。RNAGEM提取体系温和,未添加下游反应抑制成分,所以RNAGEM提取产物无需纯化。去除洗涤离心等纯化步骤,意味着降低了核酸损失率,降低引入污染和人为误差的风险,并大大减少化学试剂和塑料制品的使用。
RNAGEM工作流程比传统方法快得多,也简单得多(图1a):

图1a :RNAGEM与传统方法的工作流程对比示意图
-
准备样品(部分样品可能需要离心或匀浆)
-
将样品和试剂充分混合
-
将混合体系放入恒温设备、加热模块或水浴锅中,在75摄氏度的温度下孵育5-10分钟
-
在95℃下孵育5分钟
-
可选:添加DNAse I脱氧核糖核酸酶I,在37℃下孵育10分钟,去除提取产物中的DNA
提取流程(图1b和1c):

图1b: RNAGEM提取总核酸(DNA和RNA)工作流程
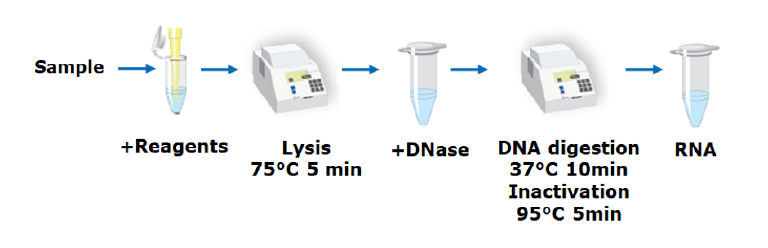
图1c: RNAGEM提取不含DNA的总RNA的工作流程
RNAGEM使用的蓝色缓冲液与聚合酶、逆转录酶及连接酶等多种核酸修饰酶兼容,因此提取产物可直接用于PCR、RT- PCR、qPCR和RT-qPCR中。
RNAGEM的实际提取体系可以根据样本量灵活调节,适用于从低至几个细胞(缩小试剂体积)或5x105细胞中(放大试剂体积)进行提取(表1)。将提取试剂直接添加到细胞样本中,从而实现96孔板高通量提取。样本量高于1x105的细胞时,提取体系可参照下表进行调整,孵育时间仍然保持10分钟。当细胞量较多时,实际最小反应体积,取决于提取终产物的粘度。粘稠是由于存在超高分子量的DNA,可以使用试剂盒提供的DNase处理,或通过涡旋、枪头反复吹打等机械力切断DNA,进而降低粘度。当细胞数较少时,实际最小反应体积仅受体系/设备蒸发限制。如果配合专门的设备,那么提取体系可以控制在1ul以内。

表1:提取体系的灵活性
【RNAGEM能有效降解RNase A】
RNA的不稳定性和对环境RNase污染敏感,是RNA提取的主要难点。即使是极少量的RNase污染也足以降解RNA。实验室RNase A污染源主要来自环境,试剂,耗材,甚至实验室用水中。传统的RNA提取方法需要仔细清洗相关耗材,以避免RNA酶污染。
图2显示RNAGEM能有效清除溶液中RNase A。在RNAGEM提取试剂中添加0.00001 - 10库尼茨单位(Kunitz unit)的RNase A,70℃孵育5分钟。孵育完成后,使用双荧光标记的RNA检测剩余RNase A活性。当RNase A存在时,双荧光标记的RNA被降解,体系荧光信号随时间增强。图中显示,在标准工作条件下,RNAGEM完全灭活高达0.1Kunitz单位的RNase A,这一数量大大超过了生物样品中RNase的预期水平,显示RNAGEM具有极好的动态范围。
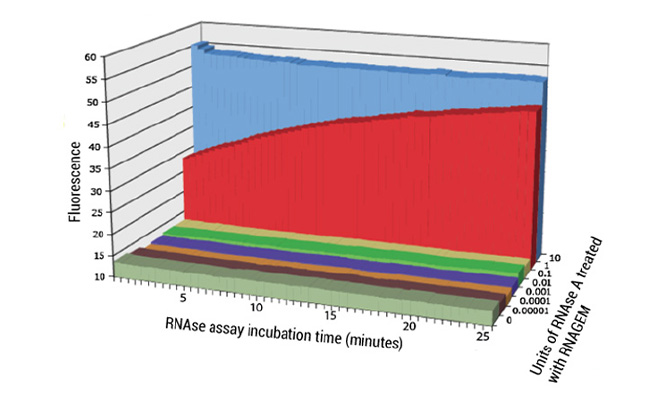
图2: RNase A梯度稀释液的残余酶活性分析。RNAGEM处理5分钟后分析溶液中RNase A残余活性。本实验设置了8种不同浓度的RNaseA溶液,范围从0Kunitz单位到10kunitz单位(如图Z轴所示)。存在残余活性时,荧光(Y轴)随时间增加(X轴)。只有从一个及以上kunitz单位的RNase A组别显示荧光随时间增加。因此,在标准提取体系中,RNAGEM可有效清除多达0.1个kunitz单位的RNase A。
【RNAGEM 、TRIzol 、RNAeasy Mini QIAGEN的方法学比较】
RNAGEM极简的工作流程保证了高核酸产量,核酸产量与起始细胞数量呈良好的线性关系。如图3所示,使用RNAGEM从HeLa细胞提取总核酸,直接取5ul提取产物进行RT-qPCR反应。如图所示,RNAGEM能从10-50,000个细胞中提取总RNA,RT-PCR法分别分析细胞中高丰度基因 (ACTB;b-actin)和低丰度基因 (BRCA1)的表达水平。如图,扩增曲线干净,梯度均匀(类似于图中红色标准曲线组)表明RT-PCR体系不存在抑制成分,而从10个细胞得到扩增曲线证明了RNAGEM的高检测灵敏性。
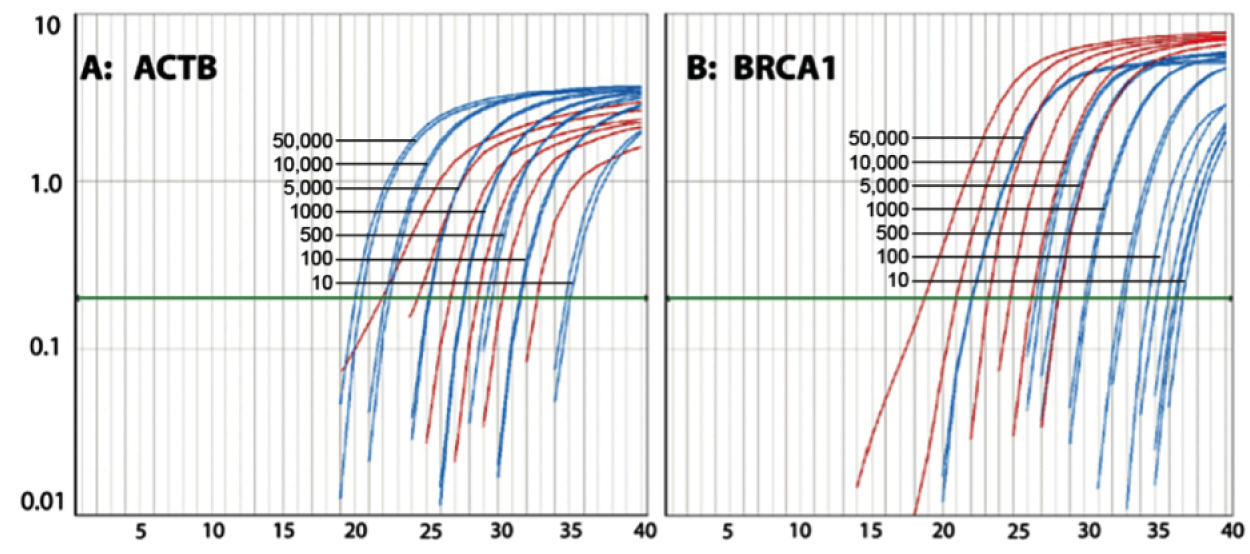
图3:从梯度稀释的10-50,000个HeLa细胞中提取RNA的RT-qPCR扩增曲线图。A: 高拷贝数基因表达分析(ACTB) B:低拷贝数基因表达分析 (BRCA1);
红色=标准曲线组;蓝色=样品组(n=2)。
RNAGEM的核酸提取效率在一个广泛的细胞数量范围保持稳定(从单细胞到~ 5 x104细胞)。图4 比较RNAGEM和TRIzol®提取方法的核酸产量。与TRIzol不同的是,RNAGEM从低到高的细胞范围内,核酸提取效率稳定,TRIzol方法则会损失RNA。从图中看TRIzol方法尤其影响样本中低丰度基因的表达量分析。RNAGEM将样本总核酸(DNA和RNA)释放到提取产物中,因此在内含子设计引物或设计跨内含子引物可以直接校正表达量。如果需要去除DNA,请使用试剂盒中提供的DNase I脱氧核糖核酸酶I。
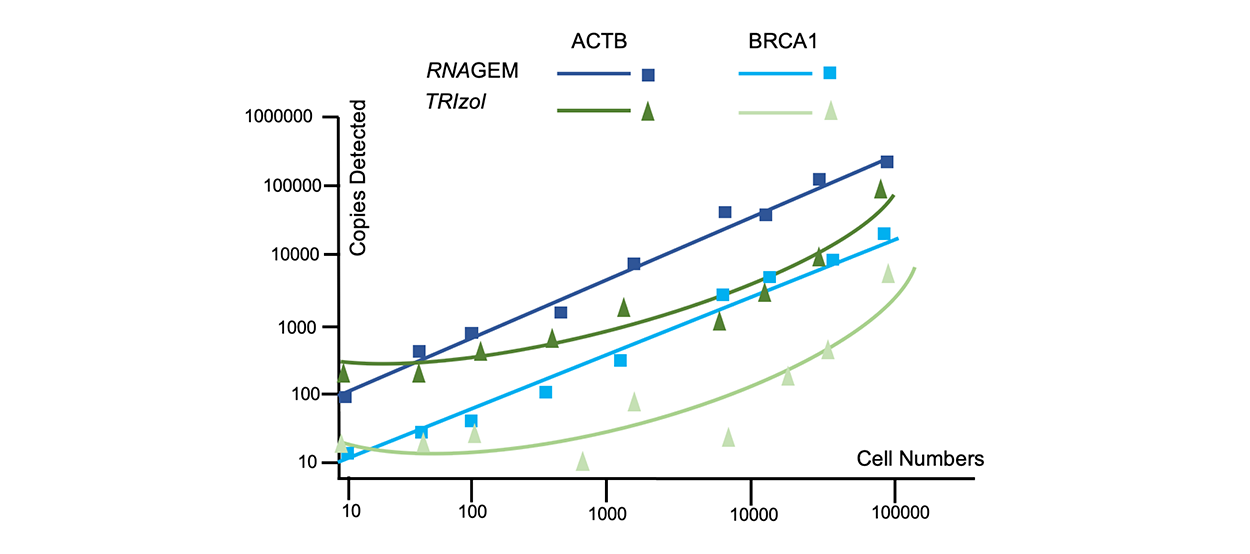
图4:HeLa细胞数量与mRNA拷贝数的对数关系图(Log/Log)。同时检测了样本中高丰度基因(ACTB)和低丰度基因(BRCA1)的表达水平。两种RNA提取试剂盒方法学比较: RNAGEM和TRIzol 。
2019年发表的一篇文章对RNAGEM和RNeasy Mini QIAGEN进行了方法学比较,以确定二者的qRT-PCR结果是否具有可比性。1文中数据显示,从相同数量的WiDr结直肠癌细胞中提取总RNA时,RNAGEM提取产物中TNFRSF11A基因表达水平是QIAGEN RNeasy Mini方法的2倍。
【RNAGEM的通用性:用于从多种样本类型中快速提取总RNA】
如表2所示,RNAGEM提取不同样本中总RNA,包括microRNA(miRNA)和非编码RNA (Inc-RNA),产物适用于多种下游应用,如PCR扩增相关应用, 环介导等温扩增技术(LAMP),Nanostring,RNAseq。RNAGEM的通用性表示其适用于多种样本类型的总RNA提取,如哺乳动物细胞培养物,激光捕获显微切割的少量细胞或组织,FACS分选的细胞群,外泌体,肿瘤组织,昆虫,细菌,病毒。

表2: 使用RNAGEM从各种样本中提取RNA的部分参考文献
Copy right 2012 by Shanghai XP Biomed Ltd. All Rights Reserved
沪 ICP备12039761号-1 沪ICP备12039761号-2 沪ICP备12039761号-3 沪ICP备13002267号-1