外泌体研究| 引领疾病治疗的新风向!
题记:继上一期小希为大家详细介绍干细胞作为细胞治疗新时代的“主角“之后,今天继续借着干细胞的光芒,为大家带来源自干细胞的外泌体知识分享。细胞治疗作为再生医学领域中新一代疾病治疗手段,已经在多类疾病研究中崭露头角,且已经有一些干细胞新药获批上市。而作为干细胞产物的外泌体在疾病治疗领域发挥出巨大潜力,已有多项干细胞外泌体治疗疾病的临床研究正在进行中。细胞治疗正在登向”大舞台“,无细胞治疗的方式已经提上日程。

外泌体必备基础知识
外泌体身份
细胞外囊泡(Extracellular Vesicles,EVs)是机体内细胞在生理和病理状态下,通过胞吞和融合作用分泌到细胞外环境中的微小囊泡,包括外泌体、微囊泡和凋亡小体。其中外泌体研究最为火热,故大家常说的EV也就特指外泌体,直径30-150 nm,内容物丰富,包括蛋白质、核酸、脂类等,可参与细胞之间的信息交流,调节细胞的生理和病理状态,以及参与许多疾病的发生发展过程。
外泌体样本来源
机体内所有的细胞都可以分泌。常规科学研究中使用的外泌体样本主要为细胞培养上清、血清、血浆、尿液、乳汁、脑脊液、卵泡液等。其中细胞上清样本占比最大,也是下游外泌体应用的重要来源。获取细胞上清样本的方法主要为:血清饥饿培养、去外泌体血清培养、无血清体系培养等。
外泌体提取方法
超离(金标准)、沉淀法+尺寸排阻色谱法(趋势)、超滤、免疫捕获等。
外泌体特征鉴定
纳米颗粒示踪分析(NTA)、透射电镜(TEM)、蛋白免疫印迹实验(WB)。
外泌体下游分析
高通量测序、蛋白组学分析、标记/示踪、功能鉴定、临床研究等。
外泌体数据文献参考
请点击阅读:“终结篇——外泌体研究合集”
外泌体与人类疾病的联系
外泌体与新冠肺炎
新冠病毒疫情仍有零星散发,形势较为严峻。通过全民接种新冠疫苗来提高整体抵抗病毒侵袭的水平,也是目前全球大部分国家采取防疫的主要方式。新冠病毒(SARS-CoV-2)可以损伤人的肺细胞,诱导分泌不同类型的炎症细胞因子,进而引发肺部损伤,导致致命的急性呼吸窘迫综合征(ARDS)。
间充质干细胞来源的外泌体被认为具有抗炎作用、免疫调节以及诱导组织再生的能力,为SARS-CoV-2诱发的肺炎提供重要的治疗机会。2020年4月,美国使用骨髓间充质干细胞(BM-MSC)来源的外泌体制品对24名SARS-CoV-2 均符合COVID-19和中重度急性呼吸窘迫综合征标准且PCR阳性患者进行单次15 mL静脉注射,并在治疗后的第1天至14天进行安全性和有效性评估。
结果显示:24例患者中,17例(71%)患者康复,3例(13%)患者病情稳定但仍处于危重状态,4例(16%)患者与治疗无关的原因死亡。总之,外泌体制品的安全性、恢复患者氧合、下调细胞因子风暴和帮助患者重建免疫的能力,有望成为重度COVID-19治疗的候选药。
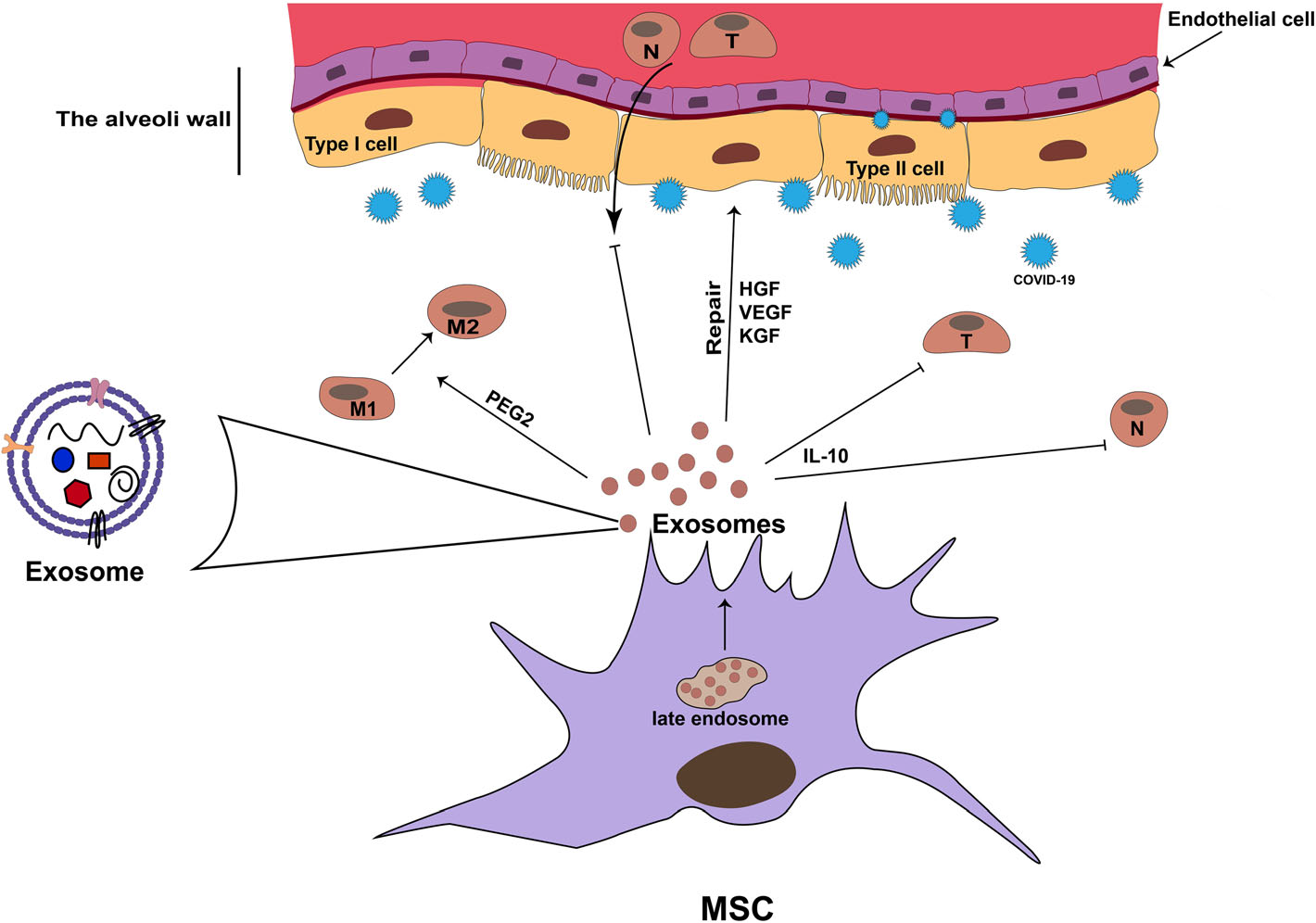
图2 MSC来源的外泌体改善SARS-CoV-2不良反应的可能机制
外泌体与肿瘤疾病
外泌体是一把双刃剑。最近的研究表明,外泌体可以参与调节肿瘤微环境,影响肿瘤的增殖和进展。外泌体已成为探索癌症疗法一个新的焦点,可用于小分子、蛋白质和RNA的治疗递送载体,以高效靶向癌细胞。
不同来源的外泌体在癌症应用中表现出多种性能。外泌体作为肿瘤微环境(TME)中最具影响的成分之一,一方面促进血管生成、增殖和转移等加速肿瘤的进展;另一方面通过免疫抑制主导树突状细胞的分化、成熟和功能的颠覆,进而阻碍抗肿瘤免疫反应的发生。外泌体被认为是疾病诊断的无创或微创生物标志物,具有检测包括癌症在内的许多病理状况的潜力。肿瘤特异性循环外泌体miRNA已被开发为肺癌的早期诊断生物标记。
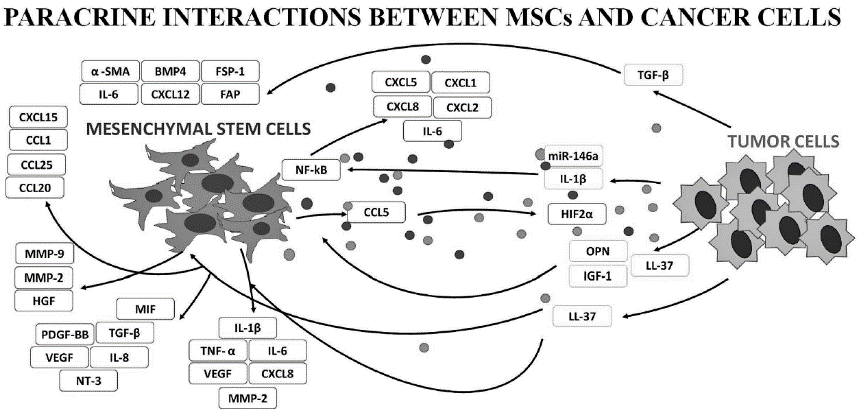
图3 MSC旁分泌与肿瘤细胞的联系
外泌体与脑部疾病
由于大脑结构与功能的复杂性,以及脑疾病发展的分子机制研究仍然处于起步阶段,给临床治疗带来很大的局限性,也给社会带来很多经济负担。
近年来,越来越多的研究开始探讨外泌体参与脑部疾病的具体机制,包括神经肿瘤、阿尔茨海默病(AD)、帕金森病(PD)、肌萎缩性脊髓侧索硬化症(ALS)、多发性硬化(MS)、亨廷顿病(HD)、朊病毒病、脑血管病、创伤性脑损伤(TBI)、精神病(抑郁症、精神分裂症、双相情感障碍、自闭症等)、癫痫症、脑膜炎等。外泌体与神经系统疾病的进展有着不可分割的联系,通过修饰外泌体以提高其靶向能力,可以改善患者的药物吸收与治疗效果。
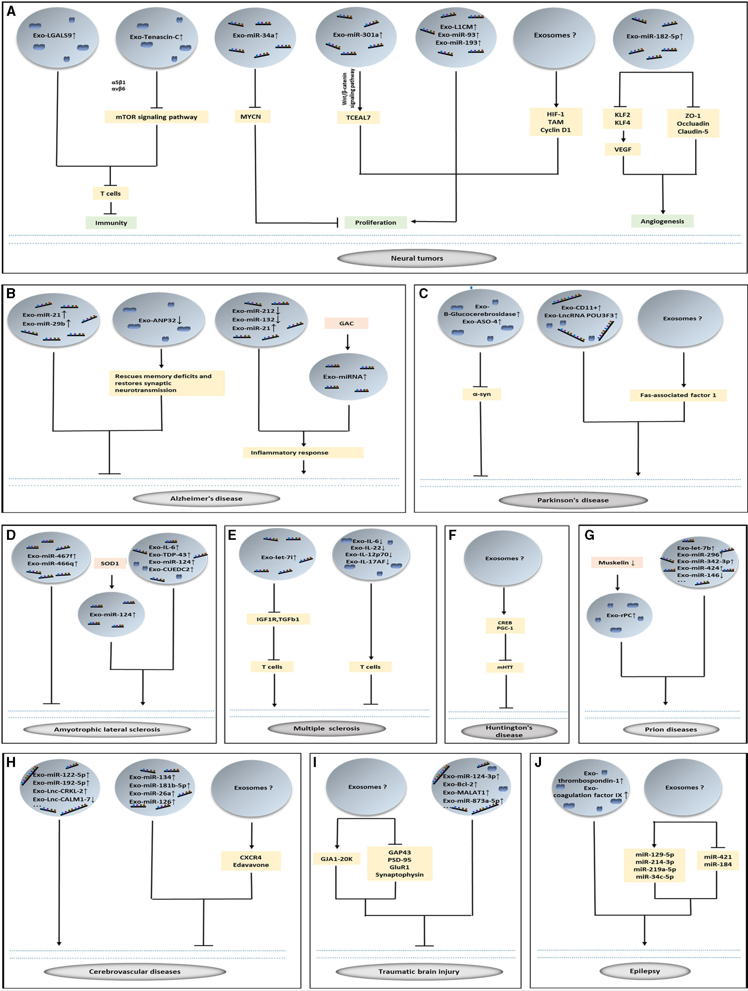
图4 外泌体与脑部疾病的联系
外泌体与自身免疫性疾病
近年来,MSCs的免疫抑制特性已在炎症和自身免疫疾病的临床前研究和试验中得到证实。新的研究证据表明,MSCs的免疫调节作用主要归因于旁分泌途径,对参与先天和适应性免疫反应的不同效应细胞有明显的抑制作用。
此外,包括多发性硬化症(MS)、系统性红斑狼疮(SLE)、1型糖尿病(T1DM)、类风湿性关节炎(RA)和炎症性肠病(IBD)等在内的自身免疫性疾病治疗也取得了实质性进展。MSC来源的外泌体能够复制MSC的功能,克服传统细胞治疗的局限性。但用于临床大规模外泌体生产的技术与程序仍有待深入探索。
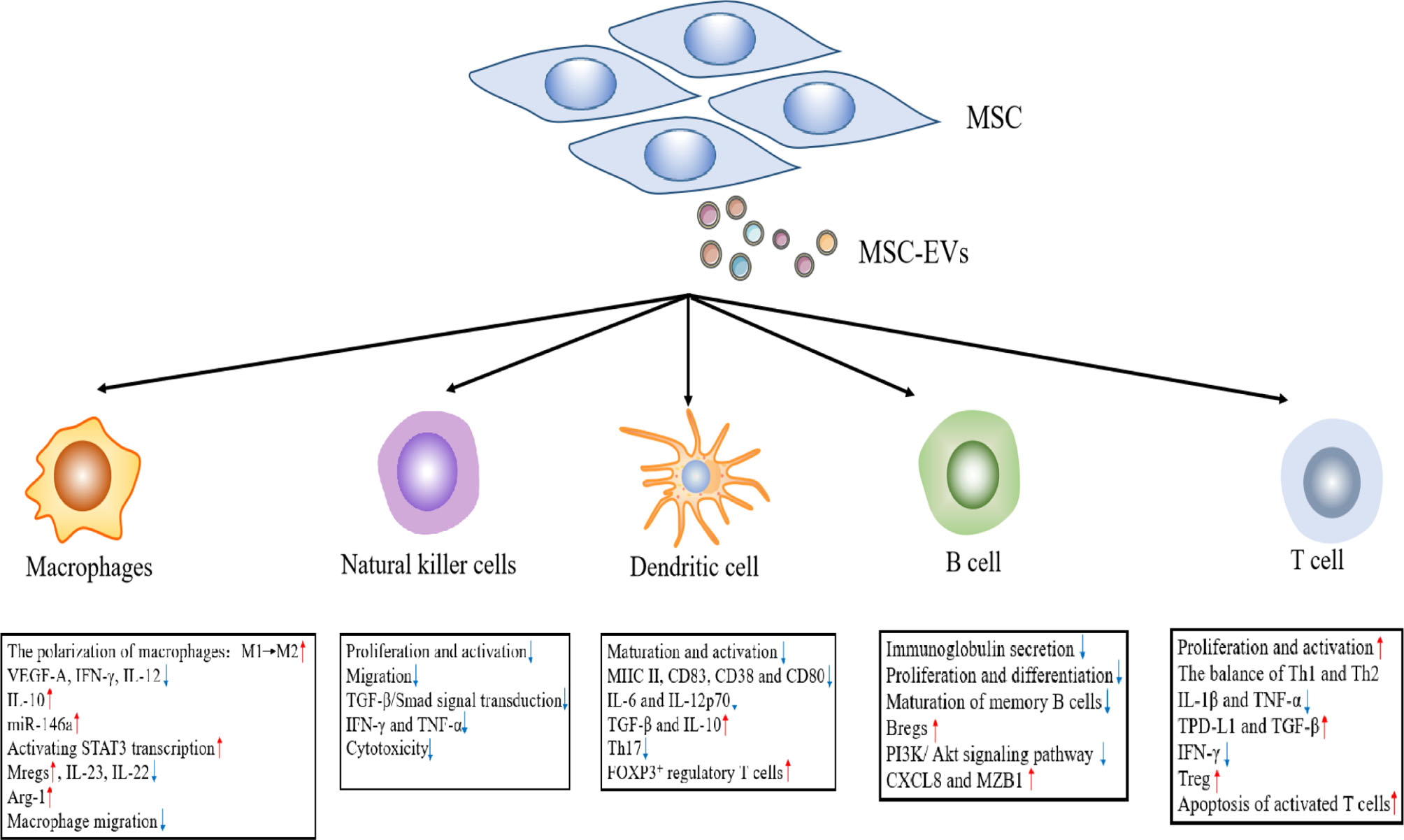
图5 MSC来源的外泌体对免疫细胞的作用
外泌体与皮肤创伤愈合
皮肤创口愈合是一个复杂的生物过程,发生在皮肤组织创伤、烧伤或糖尿病溃疡慢性皮肤创伤等是难以愈合的,是临床医生最棘手的问题之一。传统的皮肤创面护理方法有植皮、皮瓣移植、激光治疗、生物支架等,但存在瘢痕萎缩和色素异常的风险。外泌体作为细胞旁分泌的组成部分之一,避免了细胞治疗的许多缺点,外泌体稳定且易于储存,不会被系统免疫排斥,具有归巢效应,剂量易于控制等。目前脂肪干细胞来源的外泌体(ADSC-EXOs)已经成为皮肤创伤修复和治疗领域的研究热点。ADSC-EXOs应用于皮肤创伤治疗中可以调节免疫反应和炎症,促进血管生成,加速皮肤细胞增殖和再生上皮,调节胶原重塑,抑制瘢痕增生。该方法已经得到广泛的临床实践,有望实现最佳皮肤伤口愈合。
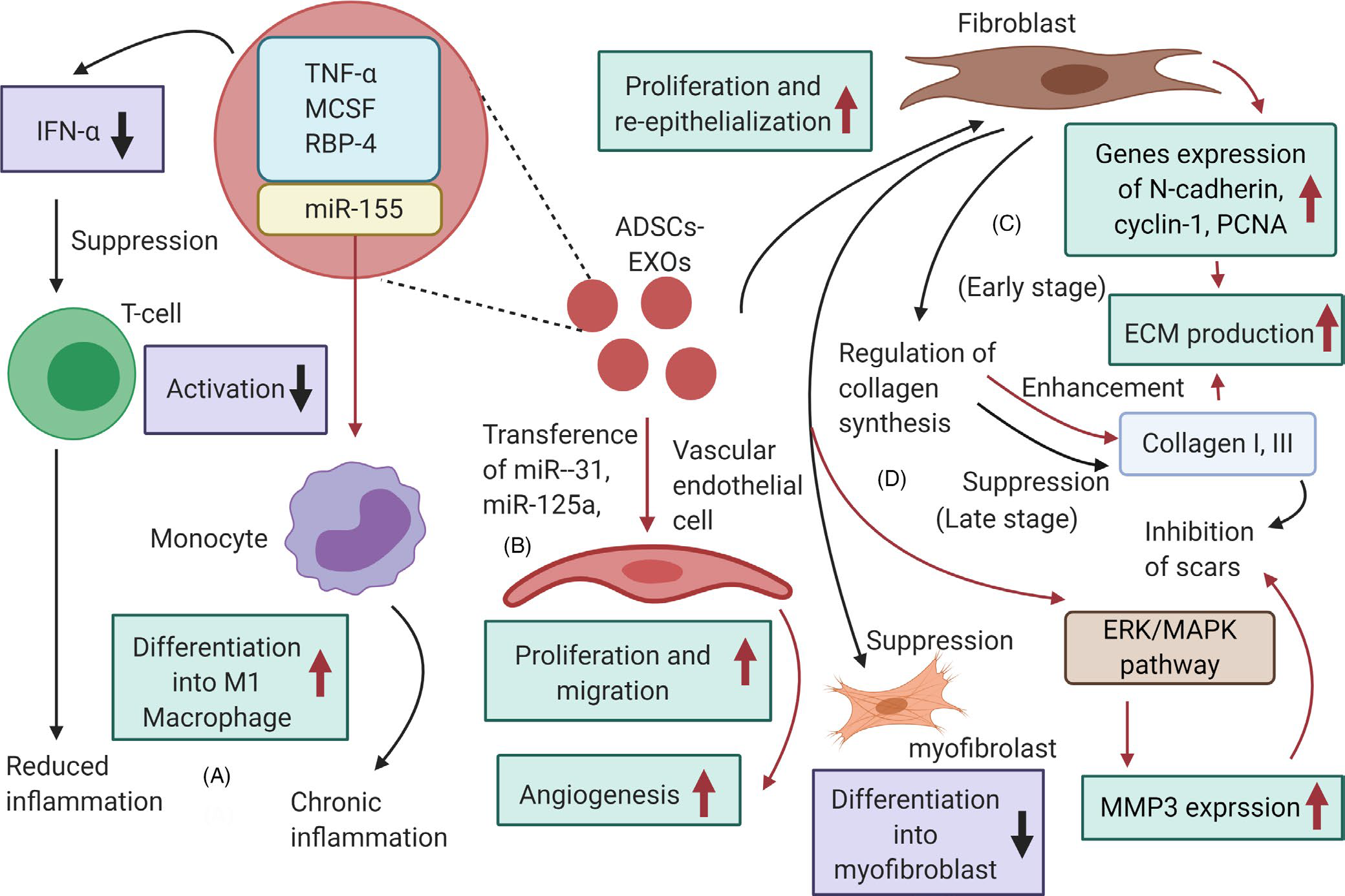
图6 ADSC-EXOs促进皮肤创伤修复的机制
外泌体,渺小而又神奇的囊泡,已经成为生命科学领域的“主角”之一。众多企业正在挖掘和开发外泌体治疗或诊断方法,针对纯天然和工程化的外泌体产品进行临床试验。国内外泌体研究相关的企业与单位不断扩增,国家相关课题基金额度也在慢慢变大,这个“蛋糕”香味已经散开了。
外泌体研究整体解决方案
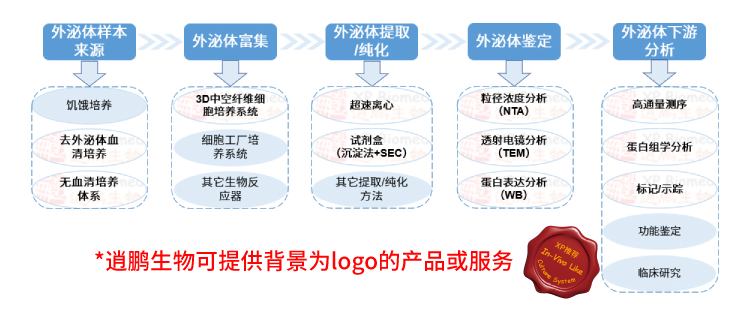
您正好需要,我正好有。从细胞培养到泌体下游分析,每一环都可以为您提供最细致的服务。逍鹏生物为您提供外泌体研究整体解决方案,更可以预约线上 “一对一”交流,助您快速掌握外泌体研究的基本知识。
参考文献
Menck K, Sivaloganathan S, Bleckmann A, et al. Microvesicles in Cancer: Small Size, Large Potential. Int J Mol Sci. 2020 Jul 28; 21(15): 5373.
Akbari A, Rezaie J. Potential therapeutic application of mesenchymal stem cell-derived exosomes in SARS-CoV-2 pneumonia. Stem Cell Res Ther. 2020 Aug 14; 11(1): 356.
An Y, Lin S, Tan X, et al. Exosomes from adipose-derived stem cells and application to skin wound healing. Cell Prolif. 2021 Mar; 54(3): e12993.
Shen Z, Huang W, Liu J, et al. Effects of Mesenchymal Stem Cell-Derived Exosomes on Autoimmune Diseases. Front Immunol. 2021 Sep 27; 12: 749192.
Zhang N, He F, Li T, et al. Role of Exosomes in Brain Diseases. Front Cell Neurosci. 2021 Sep 13; 15: 743353.
Zhou Y, Zhang Y, Gong H, et al. The Role of Exosomes and Their Applications in Cancer. Int J Mol Sci. 2021 Nov 11; 22(22): 12204.
Muralikumar M, Manoj Jain S, Ganesan H, et al. Current understanding of the mesenchymal stem cell-derived exosomes in cancer and aging. Biotechnol Rep (Amst). 2021 Jul 12; 31: e00658.
Sengupta V, Sengupta S, Lazo A, et al. Exosomes Derived from Bone Marrow Mesenchymal Stem Cells as Treatment for Severe COVID-19. Stem Cells Dev. 2020 Jun 15; 29(12): 747-754.
(部分图片来源网络)
往期回顾
Copy right 2012 by Shanghai XP Biomed Ltd. All Rights Reserved
沪 ICP备12039761号-1 沪ICP备12039761号-2 沪ICP备12039761号-3 沪ICP备13002267号-1