外泌体研究 | 您的细胞还在挨饿吗?
外泌体参与许多生物过程和病理过程,通过将蛋白质、脂质、核酸和代谢物运送到周围的细胞以及远处的器官,作为细胞间通讯的一种形式。外泌体从“垃圾”变宝的过程就在近几年,逐渐进入我们的视野,成为研究热点。
常规的细胞培养会使用动物血清,如胎牛血清,以提供激素、生长因子和其它能够支持细胞生存和增殖的蛋白质。因外泌体存在于大多数哺乳动物的体液中,如血浆、尿液和唾液中,这就意味着用于常规培养补充的胎牛血清中含有丰富的外泌体(希尔博士实验室对售卖的胎牛血清进行外泌体NTA检测,平均粒子浓度至少为1.0 x 1010 particles/mL)。据文章报道,用于科学研究的外泌体样本来源最多的是细胞培养液(超过50%),但为了减少外源性(如胎牛血清)外泌体对课题研究的干扰,以获得高质量和高纯度的细胞源性外泌体进行后续研究,目前很多研究人员选择在收获细胞上清前24-48小时将含血清的完全培养基更换为基础培养基,即血清饥饿培养法获取细胞上清。今天小希来跟大家聊一聊血清饥饿培养。
1.何为血清饥饿培养?
血清饥饿(Serum Starvation),一般是指通过降低培养液中的血清浓度,使所培养的细胞因缺乏血清中的生长因子而不能分裂,这个操作常用来做细胞同步化分裂。许多研究人员使用血清饥饿作为研究蛋白质降解、细胞应激反应、自噬、凋亡或模拟特定病理条件的分子机制研究。
2.血清饥饿对细胞的影响
血清饥饿诱导的反应迅速而动态,在不同的细胞类型和实验条件下表现出明显的定性和定量差异。血清饥饿显然是引发细胞大量不同反应的主要诱因,血清的存在或缺失可以影响细胞表型特征,影响对各种刺激的反应,甚至完全改变实验结果,因此有很大的可能干扰实验结果并影响后续结论。小希查阅文献后为您整理了几个“栗子”。
例1:mTOR通路调控细胞生长受营养物质的影响
研究发现,蛋白质合成和细胞生长受mTOR通路调控,而mTOR通路又间接依赖于营养物质、生长因子和能量可利用性(图1)。
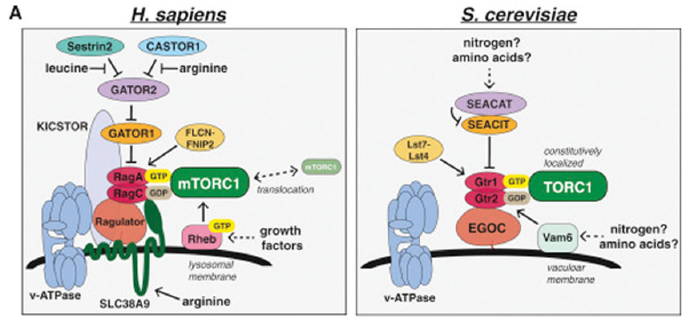
▲图1 哺乳动物mTORC(左)和酵母TORC1(右)上游的营养感应通路
例2:不同条件下细胞表达蛋白情况
Levin VA等在一项全面的蛋白质组学研究中明确显示,常规基础培养基添加10%胎牛血清可以维持细胞正常增殖,并得到不同细胞分泌蛋白水平的标准化评分(图2左)。当在含有0.5%胎牛血清的培养基中饥饿处理24h后,因对不同信号通路和肿瘤细胞类型的反应存在差异,部分细胞分泌蛋白水平的标准化评分较正常条件下发生差异性变化(图2右)。
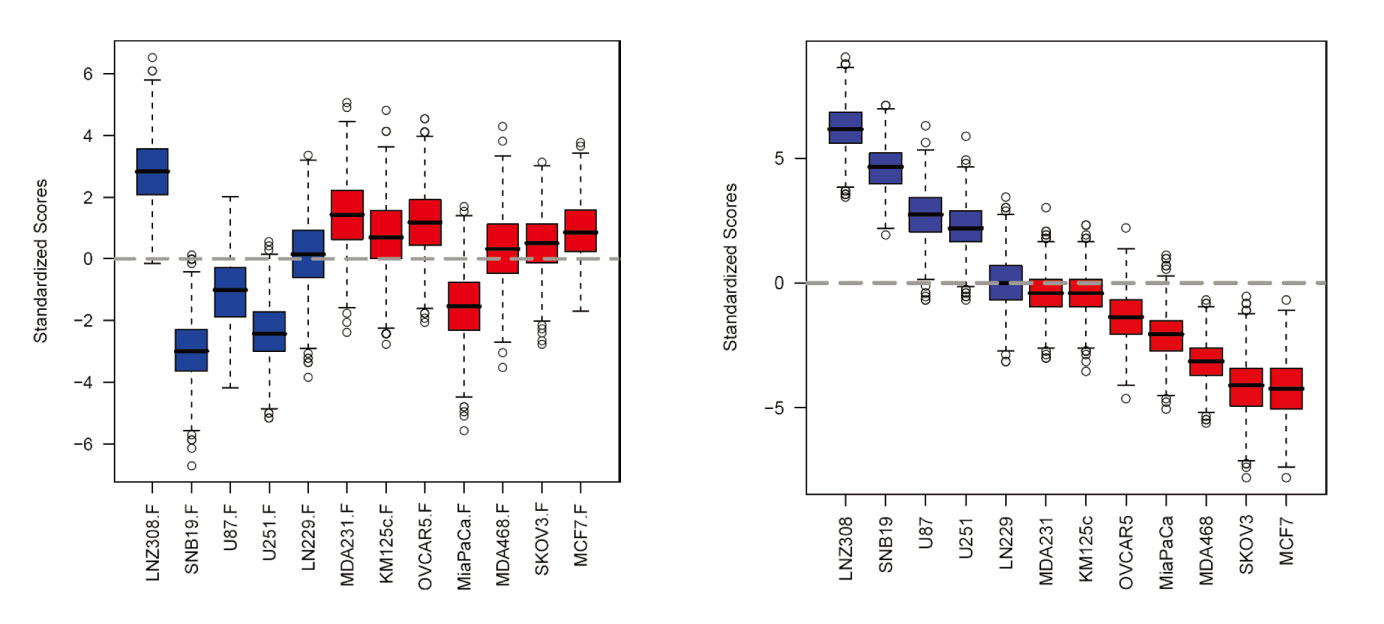
▲图2 正常血清培养条件下不同细胞表达蛋白水平的评分(左),饥饿培养条件下不同细胞表达蛋白水平的评分(右)
研究报道称,HEK-293细胞在血清饥饿培养时Caspase 3活性升高(图3)。而Caspase家族在介导细胞凋亡过程中起着重要作用,其中Caspase 3为关键的执行分子,它在细胞凋亡信号传导的许多途径中发挥功能,故Caspase 3活性升高可引起细胞凋亡。
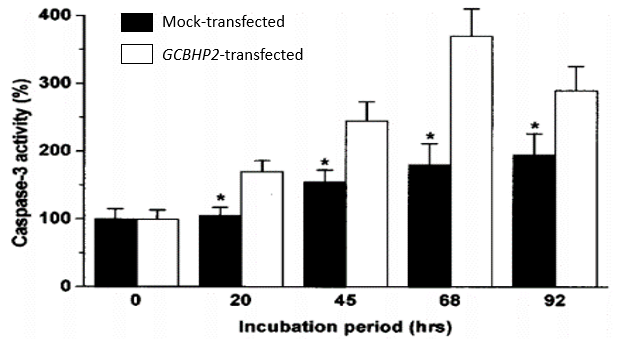
▲图3 不同血清饥饿时间下HEK-293细胞Caspase 3的活性检测
另有研究发现,血清饥饿培养导致平滑肌细胞的PDGF-β-R表达上调,IGF-1-R蛋白表达下调,分析原因可能是血清饥饿使动脉壁厚度增加,因此在动脉粥样硬化发生过程中局部影响细胞功能(图4)。
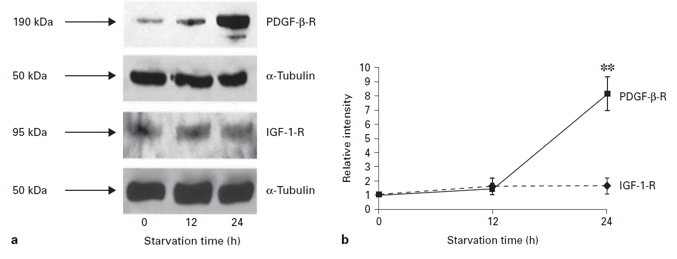
▲图4 血清饥饿对平滑肌细胞的PDGF-β-R和IGF-1-R的蛋白表达影响
例3:饥饿培养与细胞自噬的联系
Fader CM等研究表明饥饿诱导的自噬减少了外泌体的释放,作者分析由于多泡体与自噬体融合增加,从而引导多泡体进入降解途径(图5)。
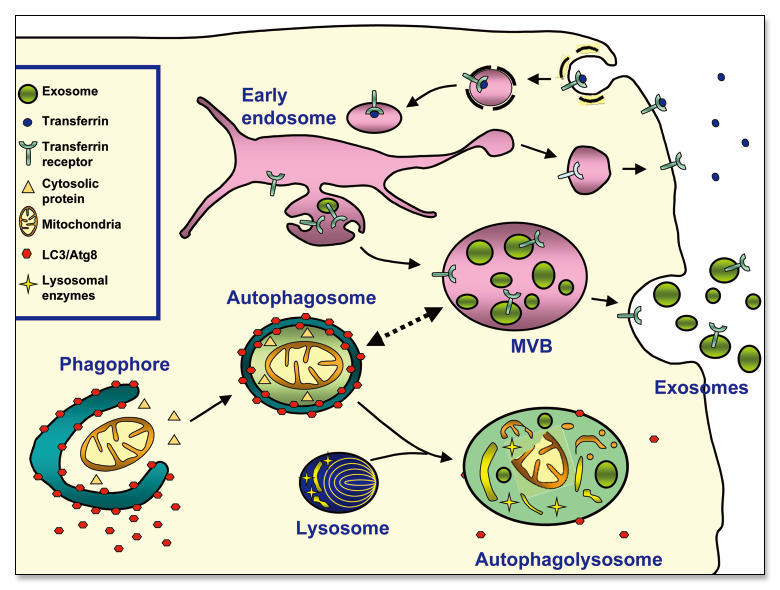
▲图5 自噬体与多泡体的联系
外泌体的一个主要作用是促进细胞的稳态,当通过血清饥饿培养来改变细胞的生长条件,会导致外泌体的蛋白质组成发生变化。当细胞发生自噬时,这种变化会加剧,也证明了外泌体和细胞自噬这两个途径是相互联系的。从细胞生物学角度来看,外泌体是研究细胞对应激反应的理想材料,因为它们可以被收集和分析。
Copy right 2012 by Shanghai XP Biomed Ltd. All Rights Reserved
沪 ICP备12039761号-1 沪ICP备12039761号-2 沪ICP备12039761号-3 沪ICP备13002267号-1